טכנולוגיה שפותחה בטכניון מאפשרת התאמה משופרת של טיפולים אנטי-סרטניים
הפיתוח, המבוסס על בינה מלאכותית, יאפשר לשפר את הטיפולים בסרטן השד ולהתריע על אבחונים שגויים
מודלים חישוביים שמפתחים חוקרים בפקולטה למדעי המחשב ע”ש טאוב יאפשרו להעריך טוב יותר יעילות של טיפולי אימונותרפיה, לנבא את תוחלת החיים של המטופל, לשפר את הטיפולים באופן מותאם אישית ולהתריע על אבחונים שגויים. את המחקר בנושא מוביל ד”ר גיל שמאי, פוסט-דוקטורנט במעבדה לעיבוד גיאומטרי של תמונות (GIP) בראשות פרופ’ רון קימל. פרופ’ קימל הוא חבר סגל בפקולטה למדעי המחשב ע”ש טאוב ופרופסור בהשתייכות משנית בפקולטה להנדסת חשמל ומחשבים ע”ש ויטרבי.
המאמר שהתפרסם כעת בכתב העת היוקרתי Nature Communications מתאר שיטה המבוססת על טכנולוגיה וניסויים שפיתח ד”ר שמאי עם אמיר ליבנה, בוגר תואר שני מהמעבדה, לצורך הערכה טובה יותר של יעילות טיפול אימונותרפי בסרטן השד. החוקרים עבדו באופן הדוק עם פרופ’ אדמונד סבו, מנהל מכון הפתולוגיה בבית החולים כרמל; ד״ר אלכסנדרה קרצו, מתמחה בפתולוגיה בבית החולים כרמל; וד״ר אנטוניו פולוניה ממעבדת הפתולוגיה Ipatimup שבפורטוגל; ובתמיכתו של פרופ׳ גיל בר סלע, מנהל המערך האונקולוגי בבית החולים העמק.
סרטן השד הפך לגורם המוות העיקרי בקרב נשים בגילאים 59-20 ולסרטן המאובחן ביותר ב-2021, עם כ-12% מכלל האבחונים ברחבי העולם. שכיחותו של סרטן השד באוכלוסייה הולכת וגדלה עקב גידול האוכלוסייה, זיהום סביבתי, תזונה מתועשת, שינויי אקלים ועוד.
מערכת החיסון מסוגלת, במקרים רבים, לחסל תאי סרטן באופן ממוקד ויעיל יותר מטיפול תרופתי. הבעיה היא שתאי הסרטן, שהתפתחו גם הם באבולוציה ממושכת, עשויים לפתח מנגנונים שמונעים ממערכת החיסון לתקוף אותם. אחת השיטות החדשניות והניסיוניות לטיפול בסרטן השד, לאור ההצלחה בטיפול בסוגי סרטן אחרים, היא אימונותרפיה – גישה המסייעת למערכת החיסון לתקוף את תאי הסרטן באמצעות פגיעה במנגנונים אלו.
אחד הטיפולים האימונותרפיים הנפוצים מתבסס על אינטראקציה של חלבון בשם PD-L1 עם תאי מערכת החיסון. האינטראקציה מעכבת את מערכת החיסון מלפעול, וטיפול אימונותרפי עשוי למנוע את האינטראקציה הזו ובכך לעזור למערכת החיסון לתקוף את הגידול. עם זאת, הטיפול אפקטיבי ומאושר לשימוש רק כאשר יש ביטוי לחלבוני PD-L1 בתאי סרטן עצמם. על רקע זה נוצר הצורך להבדיל בין גידולים המאופיינים בנוכחות החלבון PD-L1, שבהם טיפול אימונותרפי צפוי לעזור, לבין גידולים שאינם כאלה. הבעיה היא שמדידת PD-L1 אינה משימה פשוטה, ושיטות המדידה הנוכחיות יקרות ואינן מדויקות.
“לצערי חוויתי אישית את הבעייתיות של השיטות הקיימות בזמן הטיפולים האנטי-סרטניים באבא שלי,” מספר פרופ’ קימל. “אלה שיטות לא קונסיסטנטיות, כלומר – מדידות שונות של אותה תופעה נותנות תוצאות שונות. בנוסף הן יקרות מאוד ואינן זמינות בכל מקום, והתוצאה היא שהטיפולים עדיין ניתנים בתהליך שיש בו הרבה ניסוי וטעייה, כלומר בזבוז עצום של זמן וכסף וכמובן סבל מיותר.”
קבוצת המחקר התפתחה בעקבות פנייה של מתמחה (ברפואה) ששמע על נפלאות הבינה המלאכותית ופנה לפרופ’ קימל ולד”ר שמאי בשאלה: האם בינה מלאכותית תוכל לסייע באנליזה של דגימות (ביופסיה) מסרטן שד לצורך מדידת ביטוי של קולטנים וחלבונים? “ההצעה שלו נשמעה לי מעניינת מאוד והתחלתי לחקור את הנושא,” אומר ד”ר שמאי. “הלכתי לפתולוגים מומחים והם הסבירו לי שהרזולוציה של אבחון הרקמה אינה מספיקה כדי לראות קולטנים וחלבונים בלי צביעות מולקולריות מיוחדות. אחד מהם אפילו אמר שזה כמו להסתכל על דלת סגורה ולנחש מה יש בחדר. הפרויקט הזה הפך להיות המחקר שלי בשנים הבאות, כי רציתי להוכיח להם שהם טועים.” קבוצת המחקר הוקמה לפני כמה שנים ומעסיקה כיום קבוצה גדולה של מהנדסים, קלינאים וסטודנטים לתואר ראשון, שני ושלישי.
“פתולוגים שדיברנו איתם אמרו שזו משימה בלתי אפשרית,” מסביר פרופ’ קימל, “כי פתולוג אנושי אינו יכול להסיק את תכונות הגידול מתוך צורתו בגלל כמות המשתנים העצומה. החדשות הטובות הן שטכנולוגיות של בינה מלאכותית ובעיקר למידה עמוקה מסוגלות לעשות זאת. המחשב, בניגוד לפתולוג, ואפילו הפתולוג המיומן ביותר, יכול לאפיין את הסרטן בעזרת אנליזה מורכבת של המורפולוגיה שלו.”
פריצת הדרך הראשונה במחקר התרחשה לפני כשלוש שנים והוצגה במאמר בכתב העת JAMA ובו הציגה הקבוצה הצלחה בזיהוי קולטנים על גבי תאים סרטניים. הטכנולוגיה שהציגו החוקרים מבוססת על למידה עמוקה. היא מחלצת מידע מולקולרי מתוך תמונות ביופסיה שעברו צביעת המטוקסילין ואאוזין (H&E) – צביעה נפוצה המשמשת לבדיקת רקמות שנלקחו בביופסיה. הצביעה מאפשרת לפתולוג לזהות ברקמה, תחת המיקרוסקופ, את סוג הסרטן ואת דרגת החומרה שלו. עם זאת, הצביעה לבדה אינה מאפשרת לזהות חלבונים החיוניים בקביעת הטיפול המתאים. זה האתגר שעמו נדרשו חוקרי הטכניון להתמודד.
כעת, שלוש שנים לאחר המאמר ב-JAMA, מציגים החוקרים הצלחה במדידת ביטוי לחלבוני PD-L1 על מאגר דגימות גדול: ביופסיות של יותר מ-3,000 חולות סרטן שד. לדברי ד”ר שמאי ופרופ’ קימל, “למידה עמוקה מחייבת כמות אדירה של מידע, והשגת מידע מהסוג הנדרש אינה פשוטה. לצורך כך כתבנו קוד תוכנה לסריקת מקורות ברשת ולהורדה אוטומטית של אלפי דוגמאות ביופסיה ושל המידע הרפואי הרלוונטי המאושרים לשימוש מחקרי. עזרתם של הפתולוגים שחתומים על המחקר הייתה חיונית מאוד.”
המודל החישובי שפיתחו החוקרים אינו “רואה את הקולטנים והחלבונים” באופן ישיר אבל יודע להסיק את נוכחותם או את העדרם על סמך המורפולוגיה של הרקמה, או ה”חתימה” שהסרטן מותיר ברקמה, כפי שהן משתקפות בסריקות H&E. “מדובר בקשר כל כך מורכב,” אומר ד”ר שמאי, “שהאלגוריתם שפיתחנו יודע לספק לנו את המידע הנחוץ אבל אנחנו לא ממש מבינים איך הוא עושה זאת.”
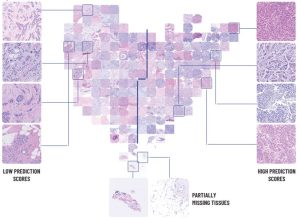
תמונה מדעית: האלגוריתם מיין את חולות סרטן השד לפי תמונות של הביופסיות שנלקחו מהן. האלגוריתם שיבץ בצד השמאלי גידולים שזיהה בהם ביטוי ל-PD-L1 ובצד הימני גידולים ללא ביטוי זה. מכאן נובע שלפי האלגוריתם, לחולות בצד ימין יועיל טיפול אימונותרפי, בניגוד לחולות שמשמאל. האלגוריתם שיבץ בתחתית מקרים שבהם לא הצליח להכריע בוודאות, ככל הנראה משום שתמונות הביופסיה לא היו טובות מספיק
המחקר מבוסס על טכנולוגיות מתקדמות של עיבוד גיאומטרי של תמונות – אחד ממוקדי המחקר במעבדה של פרופ’ רון קימל, שבמסגרתו פועלת הקבוצה של ד”ר שמאי. “זה אתגר עצום ומורכב – הפקת תמונה קלינית אמינה ומדויקת על סמך מידע חלקי,” אומר פרופ’ קימל. “יש כאן המון גורמים מעורבים – מהנדסים, קלינאים, סטודנטים ועשרה בתי חולים בארץ ובחו”ל. קבוצת המחקר נדרשה ללמוד את ההיבטים הקליניים של סרטן השד ואבחונו ולייצר מאגר נתונים עצום וכלים לניתוח הנתונים וליצירת ניבוי אמין. לגיל הייתה כאן גם משימה ניהולית עצומה, והוא עמד בה בהצלחה מרשימה, בין השאר בהשגת שבעה מענקי מחקר מקרנות שהכירו בחשיבותו של הפרויקט. למעשה הוא הקים כאן מעין סטארטאפ טכנולוגי-רפואי שמציג הישגים דרמטיים בתחום הסרטן.”
הטכנולוגיה החדשה עברה אימות (ולידציה) על נתונים מ-300 חולות סרטן השד מניסוי קליני. החוקרים מעריכים כי גישה זו, אנליזה של תמונות פתולוגיות באמצעות בינה מלאכותית, תהפוך לגורם משמעותי בחקר הסרטן, בשיפור הדיאגנוזה ובשיפור התאמת הטיפול למטופל.
המחקר נתמך על ידי רשות החדשנות (מענק קמין) ועל ידי הקרן הלאומית למדע (תוכנית המחקר ברפואה ממוקדת אישית).
למאמר בכתב העת Nature Communications לחצו כאן




