בדרך לרפואה מותאמת אישית: פריצות דרך בזיהוי החלבונים המרכיבים את התא הבודד
חוקרים בטכניון ושותפיהם בחו"ל מציגים מתווה לפריצות דרך משמעותיות בפענוח הפרופיל החלבוני של תא בודד. מאמר סקירה של קבוצת המחקר הבין-לאומית, שראה אור לאחרונה בכתב העת הנחשב Nature Methods, מתאר את הפיתוחים החדשים ביותר בתחומים אלה.
לזיהוי הפרופיל הגנטי של תאים בודדים יש ערך מחקרי ויישומי רב, וההישגים בתחום זה מסייעים להבין את השונות הרבה בין תאים שונים. עם זאת, בניגוד להצלחות בחקר הפרופיל הגנטי של תא בודד, פענוח הפרופיל החלבוני של התא הבודד היה עד כה בגדר מטרה בלתי ממומשת. מדובר ביעד משמעותי מאוד לא רק מבחינה מחקרית אלא גם מנקודת הראות הקלינית, שכן מיפוי מדויק של חלבונים מאפשר לאבחן מחלות בשלב מוקדם, שבו רמת החלבונים עדיין נמוכה מכדי להתגלות באמצעים הקיימים. מיפוי כזה עשוי לסייע גם באבחנה בין גידולים סרטניים שונים וכך להתאים טיפול אופטימלי לגידול הספציפי.
שיתוף הפעולה שהוביל למאמר הנוכחי החל בכנס בין-לאומי בראשותו של פרופ’ עמית מלר מהפקולטה להנדסה ביו-רפואית, אחד המחברים הראשיים במאמר. הכנס, SMPS19 (Single Molecule Proteins Sequencing), נערך בירושלים בשנת 2019.
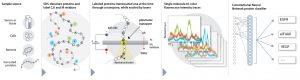
באיור: תיאור התהליך המאפשר זיהוי חלבונים ברמת המולקולה הבודדת (משמאל לימין) באמצעות ננו-חרירים. החלבונים המיועדים לבדיקה עוברים סימון מיוחד באזורים ספציפיים ולאחר מכן עוברים דרך ננו-חריר המואר באמצעות לייזר. כך מתבצעת קריאה של הסימונים השונים. האות האופטי שמתקבל מכל חלבון נקרא ונאסף ובסופו של דבר עובר לרשת נוירונים שמזהה את החלבון בסבירות הגבוהה ביותר.
במאמר ב-Nature Methods מתארים החוקרים את הטכנולוגיות העתידיות של ריצוף וזיהוי חלבונים ברמת המולקולה הבודדת לצד חידושים בשיטות קיימות כגון ספקטרומטריית מסה. מעבדת מלר בטכניון מפתחת, לדוגמה, חיישנים ננומטריים הכוללים ננו-תעלות וננו-חרירים המאפשרים חישה ישירה של חלבונים בודדים (ראו איור). החלבונים מסומנים בצבענים, וכאשר הם מוזרמים דרך החיישן, מערכת אופטית מתוחכמת קוראת את הסמנים. האות האופטי עובר עיבוד וניתוח במערכת מבוססת למידה עמוקה שגם היא פותחה במעבדה, וכך מתאפשר זיהוי החלבון. להערכת פרופ’ מלר, יכולת זאת תאפשר זיהוי וכימות של רוב החלבונים בדגימה הנבדקת והפקה של הפרופיל החלבוני של הדוגמה – לרבות חלבונים שאינם נמצאים בה בשיעור גבוה. “טכנולוגיה זאת וטכנולוגיות כדוגמתה יובילו בעתיד להבנה עמוקה יותר של תהליכים ביולוגיים ולפיתוח בדיקות רפואיות רגישות במיוחד שיאפשר אבחון מוקדם של מגוון מחלות.”
את המחקר הטכניוני הוביל פרופ’ עמית מלר ועל המאמר חתומים גם ד”ר קסנדר ון קוטן והדוקטורנט שילה אוחיון, חוקרים בפקולטה להנדסה ביו-רפואית. המחקר נתמך על ידי האיחוד האירופי (מענק ERC במסגרת תוכנית Horizon 2020 של הנציבות האירופית למחקר באיחוד האירופי), קרן המדע הלאומית (ISF) ותוכנית Azrieli fellowship.
- פרופ’ עמית מלר
- ד”ר קסנדר ון קוטן
- שילה אוחיון
למאמר בכתב העת Nature Methods לחצו כאן





